När jag tittade ut genom fönstret tidigare idag när jag var på väg ned till matsalen var allt jag såg en vit vägg. En vit vägg av is som sträckte sig både åt höger och vänster så långt ögat kunde nå (vilket inte var så väldigt långt efter som det snöade lätt och dimman, precis som så många andra dagar i det sista, envisades med att förfölja oss). Det var Dotson shelfisen, en av de mindre shelfiserna i Amundsenhavet, som majestätiskt tornade upp sig framför oss. Biologerna hade en station precis framför iskanten och ett av planktonnäten var precis på väg ner i djupet. Runt middagsbordet gick diskussionen het – hur hög är egentligen den där väggen vi ser? Tio meter? Tjugo? Trettio? Gissningarna haglade – men ingen hade svaret. Så när middagen (bläckfisk, friterad sötpotatis och ris) var avklarad gick vi upp på bron och bad kaptenen om att få låna sextanten (google eller wikipedpia kan nog förklara vad det är bättre än jag) . Medan en av matroserna letade i skåpen efter den så tog vi en titt på radarskärmen och noterade att avståndet till väggen var en halv sjömil (1 sjömil= 1852m). Innan matrosen hade hittat vad han letade efter (och innan vi lärt oss hur sextanten fungerar) var planktonnätet uppe på däck och vi var på väg till nästa station. När vi äntligen mätte vinkeln (0.77 grader) var avståndet till väggen 1.5 sjömil. Hur hög var väggen? Den som vill vara riktigt noggrann behöver också veta att bron är 16.7 meter över havet och att sextanten var 1.5 m över golvet när vi mätte vinkeln. Men skillnaden mellan att vara “noggrann” och att förenkla (det finns många sätt att göra det på) problemet är förvånadsvärt liten!

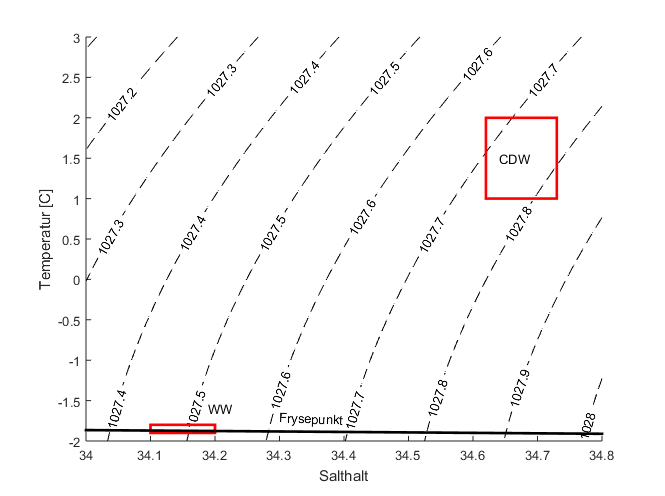
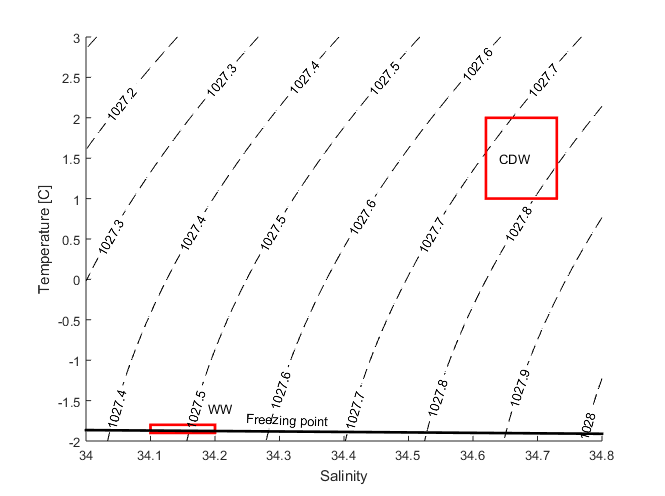
När båten stannar igen är “väggen” fortfarande där. CTD:n ska i vattnet. De koreanska oceanograferna jobbar i skift och det är alltid någon på vakt i CTD-rummet. Just nu är det Ta-wan som sitter framför den stora skärmen och knappar på datorn medan matroserna gör klar vinschen och själva CTD:n ute på däck. Det har börjat snöa igen och det blåser kallt, så jag stannar kvar i värmen inne hos Ta-wan. Radion sprakar till och jag hör några korta meningar på koreanska – samtidigt dyker det upp röda, gröna och vita linjer på skärmen framför oss, så meddelandet förkunnade tydligen att CTD:n nu är i vattnet. CTD:n får stå kvar i ytan en stund, tills pumpen (som ser till att samma vatten kommer till de olika sensorerna) har startat och allt fungerar som det ska. Sen bär det iväg ner i djupet! Graferna ritas upp “live” och linjerna på skärmen blir längre allt eftersom kabeln rullas ut och CTD:n sjunker ner. De första 30-40 metrarna är vattnet är vattnet relativt färskt (33.9) och mellan 0-0.5C; det här är ytlagret, det har blandats av vinden, värmts av solen och blivit färskt därför att det spätts ut med smältvatten från smältande havsis, snö och isberg. När vi lämnar ytlagret stiger salthalthalten till 34.2 och temperaturen sjunker till -1.5C och sen förblir både salthalt och temperatur ganska konstant i flera hundra meter. Det är “vinter vatten”, vatten som kylts av under vintern.

Tillbaka till skärmen där trycksensorn visar att vi nu nått ner till 400 m och där både temperaturen och salthalten plöstligt börjat stiga. Den blåa linjen, den som visar temperatur, försvinner till slut ut från figuren. Medan Ta-wan knappar på tangentbordet för att ändra skalan på grafen så tippar vi andra hur högt den kommer gå. När Ta-wan fått ordning på figuren kan vi konstatera att Karen och Göteborgs Universitet gått av med segern, och att det varmaste vattnet här inne vid shelfisen är 0.64 C. Det här är det varma vatten vi är här för att studera, “Circumpolar Deep Water”,som funnit vägen upp på kontinentalsockeln och strömmar söderut mot shelfisen längst botten av Dotson Trough (kanske den kan kallas Dotson Rännan på svenska/norska?), en djup ränna som isen själv grävt ut en gång för länge sen när klimatet var kallare och istäcket över Antarktis var mycket större och tjockare än vad det är i dag.
CTD:n har nått botten och framför oss på skärmen ser vi tre lager med vatten, eller tre vattenmassor, som vi oceanografer skulle kalla dem. Vattnet med lägst densitet, det lättaste vattnet, flyter överst (precis som när lätt olja flyter på tungt vattnet) och vattnet med högst densitet ligger underst. Men nu räcker det med oceanografi för i dag. Klockan blivit åtta och jag lämnar Ta-wan och de andra i CTD-rummet och beger mig upp till träningsrummet och pingisbordet. Povl (en dansk oceanograf som sedan många år jobbar på British Antarctic Survey i Cambridge, UK) och jag har blivit utmanade av Monsieur Park och Isabelle från L’Ocean i Paris, så här gäller det att kavla upp ärmarna och försvara de skandinaviska färgerna!

Ps – medan vi var uppe och spelade pingis så satte Nicole (från Rutgers University, USA) en “glider” i vattnet. Glidern kan ändra sin volym (och därmed sin densitet, eftersom massan inte ändras) och med hjälp av sina vingar kan den, fullastad med sensorer, därmed flyga upp och ned i vattnet. En självgående CTD, helt enkelt! När den är uppe i ytan skickar den hem data och position via sateliter, och den kan också ta emot nya order om vart den ska simma, hur djupt den ska dyka, och vilka sensorer som ska vara på. Om ni går in på www.marine.rutgers.edu/cool/auvs och letar efter glider RU25 så kan ni se vad glidern har gjort och vad den samlat in för data!

Ps 2 – Skandinavien vann!
Oppgaver og øvelser
Norsk
- Saltholdighet, temperatur og tetthet.
- Bland en lagdelt drink
- Bygg et «vanntermometer»
- Hvor mye salt er det i havet?
Svenska